timsOmni™同时具备timsTOF的速度和性能以及新型Omnitrap的功能。以前所未有的深度和速度助力完整蛋白的深度测序和翻译后修饰的精准鉴定与定位,助力突破蛋白质组学限制,解锁蛋白变体世界奥秘,以全新科学视角点亮功能性、治疗性及病理性蛋白质异构体的探索之路。
1.timsOmni™提供“瑞士军刀”般的灵活性,支持基于电子和碰撞诱导的碎裂技术,为下一代蛋白质变体研究提供更多可能性,推动疾病研究、生物制剂开发与先进的生物工艺质量控制
2.基于Omnitrap快速、灵敏和多样的MSn功能进一步丰富了完整蛋白水平研究内容,能够准确识别磷酸化、糖基化等关键的修饰信息,实现蛋白序列的深度覆盖,获得结构信息
3.通过精准调控电子捕获和电子诱导解离模式(eXd)的电子能量,以超高的灵敏度实现高达100%的序列覆盖率,准确揭示H3组蛋白乙酰化修饰位点信息
4.支持碰撞诱导去折叠(CIU)功能,结合eXd之前TIMS获得的碰撞横截面(CCS)数据,精确捕捉蛋白构象转变过程
5.OmniScape™蛋白测序分析软件:基于机器学习的先进去卷积和评分系统,实现高置信度的蛋白质变体鉴定、蛋白质从头测序、PTM鉴定定位和复杂糖基化分析
6.具备timsTOF平台超快的扫描速度和灵敏度,支持微量样本的bottom-up高灵敏度4D-蛋白质组学
重大飞跃:实现深度蛋白质变体测序
深度测序
独特的 Omnitrap® 平台设计,通过利用多级 MSn eXd 工作流程实现离子富集和信号放大,体验无与伦比的全扫描 MS 和MSn 灵敏度。
电子能量控制
解锁更宽的电子能量范围,并利用 Omnitrap® 技术的多模态和 eXd 捕获技术能力,全面测序您的目标蛋白质。
准确性
利用 TIMS 分离获得准确的 CCS 值,以确定构象异构性,并使用碰撞诱导去折叠(CIU)来深入了解蛋白质的二级结构。
多功能性
基于经过验证的 timsTOF Ultra 2 平台,原有 PASEF® 模式继续支持 Bottom-up 分析,同时搭载完整的 Omnitrap® 工作流程以进行完整蛋白质分析。
timsOmni™ 凭借 eXd 技术和 TIMS 的强大优势,实现复杂结构解析和深度蛋白质变体测序。 创新融合多项技术优势,提供无与伦比的功能多样性。
• TIMS 提供精确 CCS 值,解析构象异构性
• 碰撞诱导去折叠(CIU)以探索生物分子的构象全景
• 精确控制电子诱导碎裂(eXd),实现详细的分子特征分析
• 多维MSn 分析结合离子富集技术以实现无与伦比的灵敏度
• 捕获 eXd 模式,优化前体离子利用率,提高碎片离子产率
• 全面支持所有 PASEF® 模式进行 Bottom-up 蛋白质组学和多组学研究
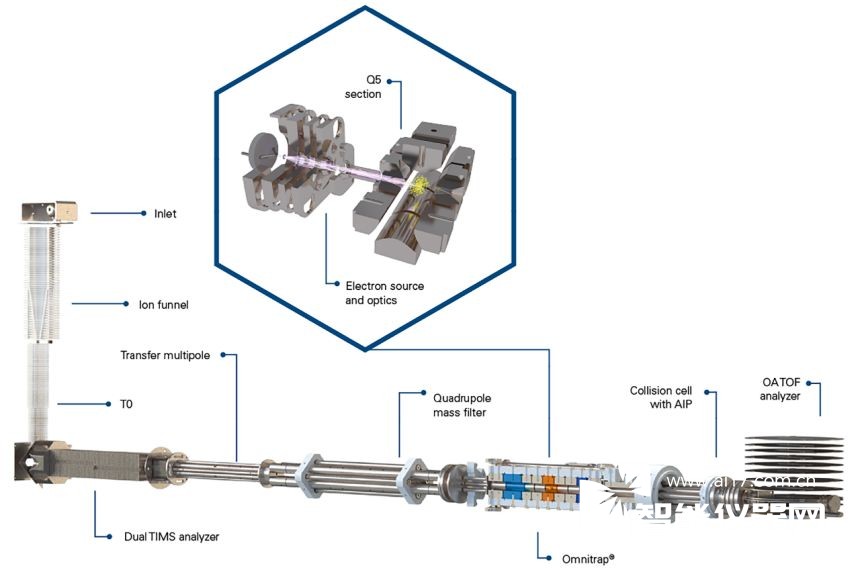
体验无与伦比的 MS 和MSn 灵敏度
timsOmni™ 通过多维度 MSn 分析和离子富集,提供无与伦比的全扫描 MS 和 MSn 灵敏度,即使对于丰度极低的离子也能显著放大信号。
得益于多级 MSn eXd 工作流程,通过精确控制离子束,任意强度的离子均可被靶向进行电子诱导解离。
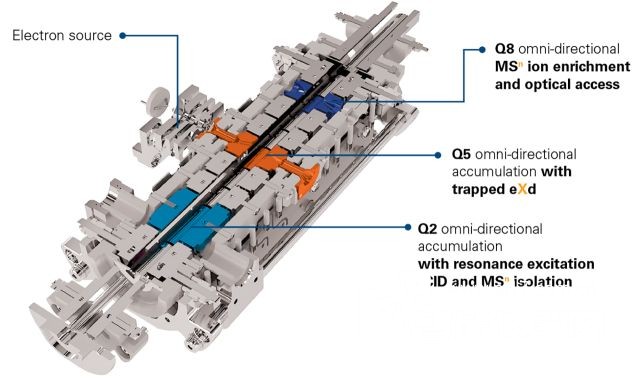
精确调节电子能量和反应时间
timsOmni™ 能够精确调谐电子能量,从而探索多种碎裂模式,并灵活调整 eXd 反应时间以获取理想结果。凭借获取的完整电子碎裂谱图,您可以设计全新的解决方案,以实现深度测序和详细的结构解析。
捕集 eXd 模式
在 eXd 捕获模式下,前体离子被捕获并在电子辐射下快速碎裂。通过调整捕获时间,可显著提升碎片产率,优化前体离子消耗率(> 90%)。这种独特的碎裂功能与传统的单一能量和固定反应时间的碎裂技术截然不同。
Charge DDA算法用于完整蛋白分析
Change DDA(cDDA)算法在 LC-MS 分析过程中实时进行电荷状态去卷积,从而实现对宽动态范围内共流出蛋白质变体的精确靶向分析,有效避免高丰度蛋白的冗余碎片。 通过动态地将隔离窗口切换到 m/z 谱图的非重叠区域,cDDA 显著减少了混合谱图的产生。
抗体互补决定区测序
分析和监测健康个体和需要治疗的患者体内的抗体水平对于表征疾病进展、识别症状发作延迟的患者以及预测潜在的长期免疫至关重要。
• 全面丰富的碎片信息对于表征抗体独特的互补决定区(CDRs)至关重要。CDRs 是位于轻链和重链可变区内的主要高度变异环,主要负责抗体对特定抗原的选择性和亲和力。
• CDR 测序是指识别这些环中确切氨基酸序列的过程,以确认抗体身份、评估潜在突变或促进抗体开发应用。
CDR 测序的卓越 eXD 效率得益于以下几点:
• 高容量 eXd 区,单次扫描可存储并处理 > 1000 万电荷
• 高亮度电子源,精细能量控制,加速 eXd 反应
• 精确控制 eXd 反应时间,确保前体离子最大利用率
• 增强二级谱图信噪比,实现最大序列覆盖率
赋能深度表征:MSn 负离子模式下的寡核苷酸分析
DNA 和 RNA 对于维持细胞稳态至关重要,它们驱动蛋白质翻译并通过表观遗传学和干扰RNA等机制调控基因表达,现正日益广泛地作为重要药物形式应用于多种疾病治疗领域。 表征内源性 RNA 修饰对于理解生物过程至关重要。然而,由于核苷酸种类有限以及甲基化等同位素修饰的存在,对这些分子进行精确表征仍然具有挑战性。 寡核苷酸带有负电荷,其表征需要采用特殊的断裂技术,因为尽管标准核苷酸种类有限,但可能存在多种修饰。定位内源性 RNA 修饰是理解生物过程的关键,而结合 timsOmni 技术的完整蛋白质组学分析能够实现精确测序。MSn eXd 技术可执行电子脱离解离(EDD),特别适用于寡核苷酸类治疗药物的完整蛋白质表征。
解析疾病机理的关键 —— 组蛋白乙酰化
组蛋白在 DNA 组装中起着关键作用,组蛋白乙酰化通过改变染色质结构在基因表达调控中发挥重要作用。 理解组蛋白乙酰化是理解癌症、神经退行性疾病、心血管疾病或代谢紊乱的基础。组蛋白结构中修饰位点的高变异性要求数据解析工具必须能提供可靠的分析结果,timsOmni™ 最先进的碎裂能力结合 OmniScape™ 软件的智能算法,能够实现高置信度的 PTM 位点匹配
Omnitrap 多模态和多级 MSn 技术推进应用蛋白质组学领域创新发展
细菌酶凭借其卓越的效率、特异性和经济高效的生产方式,正在彻底改变工业生产流程。 在食品制造领域,这些酶通过分解淀粉、蛋白质和果胶来促进发酵、改善质地并优化产品。 在制药制造领域,高效酶可简化药物合成,从而提高产量并改善产品质量。
突破 native MS,实现蛋白质复合物的深度测序和翻译后修饰(PTM)表征
理解膜蛋白如何在健康和疾病状态下组装以发挥功能对于药物开发至关重要。这需要对蛋白质低聚态、亚基相互作用、翻译后修饰及其与配体和抑制剂的结合进行多层次分析。 新型 NEOS-Source 离子源专为完整蛋白分析设计,增加喷雾稳定性和实验重现性。
MSn eXd:小分子高级结构解析利器
氯原子在哪里? 芳香族氯通常不具反应性,广泛存在于许多药物中;而苄基氯则是对 DNA 和蛋白质具有强效烷基化作用的试剂,使其具有致癌性。因此,在痕量杂质中确定氯化位置至关重要,因为苄基氯必须受到严格控制,以最大限度地降低其致突变性。 timsOmni 超越了目前可用的 MSn CID 和 MS2 EID 激活方法,通过 MSn eXd 技术触及以前无法到达的分子键,从而解决这类关键问题。
监测体内生物转化产物以提高生物治疗的疗效
多特异性抗体作为一种领先的生物治疗类别正在迅速崛起,能够同时结合多个靶标抗原。这些创新的模式提供了新的作用机制,增强了疗效,降低了耐药风险,并且与传统疗法相比,副作用更少。然而,与单克隆抗体不同,多特异性抗体在体内更容易降解,需要通过代谢物特征进行彻底分析。 完整蛋白分析和 Middle-down 的质谱(MS)方法特别适合这种详细的结构分析,因为 Bottom-up 的策略往往无法获取完整的蛋白结构信息。这一挑战更加复杂的是,这些代谢物在体内样本中的浓度极低,这使得它们的分析特别困难。引入 timsOmni 标志着一个重大进步,开启了全面表征多特异性抗体模式的新纪元。













